De Verenigde Staten heeft de grootste afzetmarkt voor medische hulpmiddelen wereldwijd. Hier komt de FDA en de Food & Drug Administration om de hoek kijken. Zij stellen specifieke eisen rondom de effectiviteit en veiligheid van medische product. De praktijkgerichte training Markttoegang voor medische hulpmiddelen volgens FDA regelgeving leert je hoe een medisch product in de VS op de markt brengt
- Ontdek welke eisen er worden gesteld aan elektronische bestanden, software- en procesvalidatie, medische hulpmiddelen rapportage, terugroepacties en Kwaliteit Systeem Inspectie Techniek (QSIT-guidance)
- Leer te werken volgens de Quality System Regulation (21 CFR 820)
- Ken de regelgeving en begeleiding voor risico beheersing
Over de training Markttoegang voor medische hulpmiddelen volgens FDA-regelgeving
Steeds meer bedrijven richten hun pijlen op de Verenigde Staten vanwege de enorme groeipotentie voor het op de markt brengen van medische hulpmiddelen. Wil je een product daar op de markt brengen, dan moet deze voldoen aan de eisen van de FDA: de Food & Drug Administration. De training Markttoegang voor medische hulpmiddelen volgens FDA-regelgeving maakt je wegwijs in het voldoen aan deze eisen.
De ruime ervaring van de docent met de FDA maakt deze training een aanrader voor iedereen die op zoek is naar een gedegen inzicht in de FDA regelgeving en handvatten om te voldoen aan de eisen. Na afloop van deze training weet je hoe te werken volgens de Quality System Regulation (21 CFR 820), de regelgeving, begeleiding en risico beheer. Maar ook welke eisen er worden gesteld aan elektronische bestanden, software- en procesvalidatie, medische hulpmiddelen rapportage, terugroepacties en QSIT-guidance voor FDA.
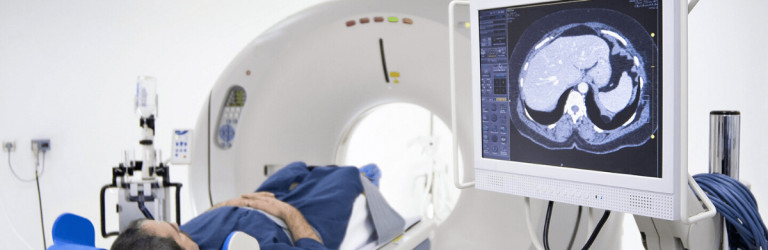
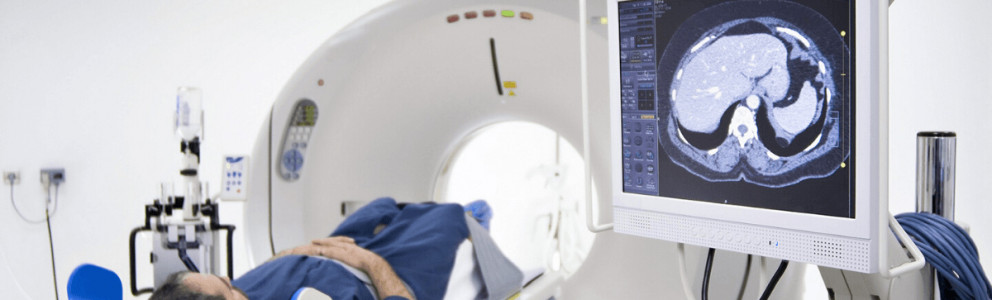
Programma
Tijdens de training Markttoegang voor medische hulpmiddelen volgens FDA-regelgeving komen de volgende onderwerpen aan bod:
Verenigde Staten versus Europa
- Kort historisch perspectief en nieuwe ontwikkelingen
- FDA versus Notified Bodies
- Samenwerking tussen FDA en Notified Bodies
Vrijgaveroutes voor markttoetreding
- Premarket Approval (PMA), 510(K) submission, De Novo-route
- Relatie met de Europese richtlijnen (MDR en AIMD)
Eisen aan het kwaliteitssysteem
- 21CFR 820: Quality System Regulation
- Specifieke wetgeving in relatie tot Quality System Registration (QSReg): zoals Unique Device Identification (UDI), volgsysteem, correcties en terugtrekking
- Ontwerp verificatie en ontwerp validatie
- Proces kwalificatie en validatie
- Software validatie en 21CFR 11 (elektronische bestanden & handtekeningen)
- Relatie met ISO 9001, ISO 13485 en ISO14971
Hoe audit de FDA een kwaliteitssysteem?
- De Quality System Inspection Techniques (QSIT)
- Do's en don'ts tijdens een FDA-audit
Samenvatting van FDA-eisen en voornaamste verschillen/overeenkomsten met Europese-eisen.
Neem contact op voor meer informatieErvaringen van cursisten
Plaats, data en prijzen - Open inschrijvingen
Inschrijven
Plaats
Startdatum
Begintijd
Eindtijd
Prijs
Avonden / Dagen
Mikrocentrum werkt met all-in-prijzen. Alle genoemde bedragen zijn exclusief B.T.W. en inclusief lesmateriaal en arrangementskosten.
Leden van het Mikrocentrum High Tech Platform ontvangen 10% korting op de cursusprijs.
Ontdek de mogelijkheden om deze training bedrijfsintern te organiseren
Wanneer je meerdere medewerkers in jouw bedrijf op wilt laten leiden, is het interessanter en voordeliger om een cursus bij je op locatie te organiseren. Een goede afstemming op jouw bedrijfsspecifieke situatie en de inzet van zeer ervaren docenten die hun sporen in de praktijk hebben verdiend is hierbij essentieel. Mikrocentrum is CEDEO-erkend en garandeert de beste kwaliteit.
Onze programmamanager opleidingen denkt graag met je mee!
Heb je interesse in een bedrijfsintern traject? Onze programmamanager opleidingen Barend Blom komt graag vrijblijvend bij je op bezoek.